据全国多家医院统计数据显示,春节长假过后,约有30%至40%的肿瘤患者出现了病情恶化的情况。这一现象可能与节日期间的生活不规律、对病情的忽视等因素有关。
癌症的复发和转移,主要归因于其快速生长和高度扩散的特性。同时,治疗不彻底、免疫力下降等因素也可能对癌症的复发和转移产生影响。这提醒我们在节日期间也应保持健康的生活方式,并密切关注身体状况,以预防病情恶化。
1
肿瘤转移的四种途径
恶性肿瘤的转移主要有四种方式:
局部扩散,即肿瘤的直接蔓延;
淋巴管渗透,指癌细胞从局部淋巴管扩散至整个淋巴系统;
血行转移,即癌细胞随血流到达身体的其他组织器官;
种植转移,发生在肿瘤细胞脱落后在体腔内流动,并在其他器官表面定植形成新的转移灶。
在预防和控制癌症复发方面,人体免疫力发挥着至关重要的作用。免疫细胞治疗作为一种方法,有助于重建免疫系统,进而增强身体对癌症的抵抗力。现代医学研究显示,恶性肿瘤患者的免疫系统往往功能失调,无法有效清除异常细胞,这导致了肿瘤细胞的增殖。而免疫系统的功能恢复是促使癌症减退的关键因素之一。
临床上的研究进一步证实,癌症治疗的效果约有一半依赖于药物,而另一半则取决于患者自身的免疫力。当免疫功能低下时,即使使用了高效药物,其治疗效果也会大打折扣;相反,若免疫系统处于正常状态,药物治疗的效果会更加显著。这强调了免疫力在癌症治疗中的重要性。
免疫细胞治疗,作为一种前沿的癌症疗法,旨在激活并增强患者自身的免疫系统,从而利用免疫系统自身的力量来消除癌细胞和组织。这种疗法对多种实体瘤,包括肺癌、肝癌、乳腺癌和食管癌等,都展现出了显著的治疗效果。
在癌症的放化疗阶段,免疫细胞治疗能够调整免疫系统,激活并修复受损的免疫细胞,促进免疫因子的分泌,进而重建免疫防线。这不仅能有效抑制肿瘤细胞的增生,还能减轻放化疗带来的毒副作用。对于晚期癌症患者,手术后结合化疗和免疫细胞治疗,可以有效清除残余的癌细胞,降低复发和转移的风险。
免疫细胞治疗的方法是从患者的外周血中分离出免疫细胞,然后在特定的培养基中进行培养,以扩增细胞数量。这些扩增后的细胞最终会被重新输注到患者体内。其中,NK细胞在肿瘤免疫监视中扮演着关键角色,它能够在不事先致敏的情况下摧毁异常或癌细胞。
NK细胞通过识别细胞表面主要组织相容性复合物(MHC)I类的异常表达来区分正常细胞和异常细胞。它能通过多种机制,如释放导致细胞凋亡的穿孔素和颗粒酶、与死亡受体配对以及分泌不同的效应物质等,来消灭癌细胞。
随着对NK细胞生物学和功能的深入研究,它已经成为癌症免疫治疗中的有力武器。尤其对于那些在一线治疗或维持治疗中效果不佳的癌症患者,结合免疫细胞治疗往往能带来令人鼓舞的治疗效果。
非小细胞肺癌(NSCLC)作为最常见的肺癌类型之一,长期以来一直是全球健康领域面临的重要挑战。然而,2022年12月,《Respir Med Case Rep》杂志公布的一份病例报告为NSCLC患者带来了新希望。报告详细记录了一位NSCLC复发患者接受免疫细胞治疗后的显著效果。
在接受免疫细胞治疗后,患者的临床症状得到了明显改善,生活质量也有了显著提升。更令人振奋的是,治疗后仅6个月,患者的原发肿瘤大小减小了近一半,这一成果充分证明了免疫细胞治疗在NSCLC治疗中的巨大潜力。
02
案例报告
2019年5月,一名60岁的男性患者,无吸烟史,出现咳嗽、背痛和疲劳症状,被诊断为非小细胞肺癌(NSCLC)。CT显示左肺上叶有一个主要肿瘤,大小为25×31毫米,侵犯纵隔组织,紧邻主动脉(图1A)。纵隔中可见数个淋巴结,最大的尺寸为5×15毫米,而右肺上叶显示两个分别为5毫米和7毫米的淋巴结。
通过CT引导下经皮穿刺活检的结节和腺癌组织经病理学检查确认(PHE)。病理分期为T4N2M1a(第四期)。肿瘤标志物CA125轻微增高(55U/ml),CA199和CEA均在正常范围内。分子分析显示EGFR无突变。由于病变较大且侵犯纵隔,无法进行手术治疗。
图1. 初次诊断时的主要肿瘤CT扫描检查(A)。在第一线治疗后(卡铂650毫克(AUC5)加上紫杉醇300毫克(175毫克/平方米),与放疗联合治疗,共3个周期),主要肿瘤PET/CT扫描检查(B)。
从2019年6月到2019年12月,患者接受了首次治疗,即卡铂650毫克(AUC5)加上紫杉醇300毫克(175毫克/平方米),第三个周期联合放疗。他出现了部分缓解,临床和辅助检查症状都有所改善。患者的正电子发射断层扫描(PET)/CT显示主要肿瘤大小减小至12×7毫米(图1B),肿瘤标志物值在2019年12月恢复正常。
然而,疾病在2020年5月出现了局部进展。PET/CT扫描显示主要肿瘤大小为28×29毫米(图2A),最大标准摄取值(SUVmax)为11.2,与纵隔胸膜和主动脉粘连。此外,左锁骨上淋巴结出现大小为9×6毫米(图2B),左肺门还有几个直径小于10毫米的小淋巴结。
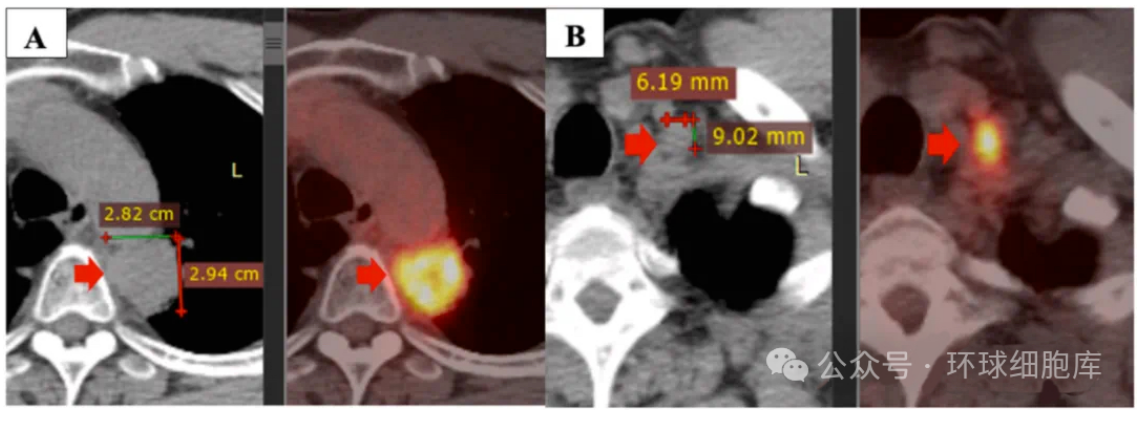
图2. 在首次治疗一年后疾病出现进展:主要肿瘤(A),左锁骨上淋巴结(B)。
患者显示出阳性的PD-L1表达(25%),被建议接受第二线治疗,包括4个周期的艾美单(500毫克x2)、卡铂(150毫克x2,450毫克x1)和凯特鲁达(4毫升x2)。然而,患者的病情在2020年9月PET/CT扫描随访中发现进展。主要肿瘤增大至26×35毫米(SUVmax:22.6)(图3A)。此外,还出现了新的病变,如右锁骨上淋巴结、前纵隔和气管旁的淋巴结,以及两侧肺门区的少数淋巴结。由于病情进展,患者的治疗方案发生了变化。2020年10月,患者被住院进行自体NK细胞输注,共接受6次输注,与吉西他滨/阿瓦斯汀联合治疗。入院时,患者无发热,脉搏为每分钟79次,血压为110/70毫米汞柱。他经历了干咳和左胸闷痛。辅助检查结果包括血液学和血液生化均正常,除了白细胞计数偏低(2.81 G/L,低于正常水平)。
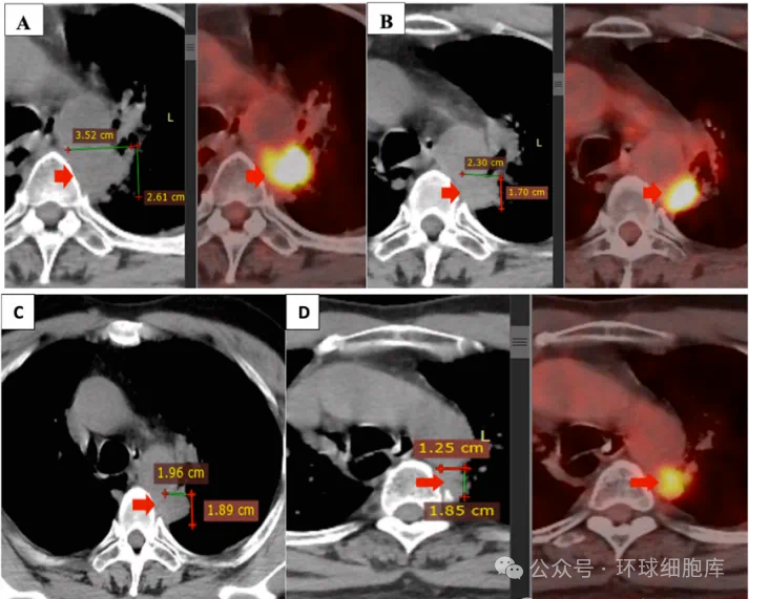
图3. 联合治疗前后的主要肿瘤情况。二线治疗(4个周期的艾美单、卡铂、凯特鲁达)后,主要肿瘤进展(A)。在自体NK细胞治疗、吉西他滨和贝伐单抗联合治疗结束时,主要肿瘤缩小(B),3个月后(C),6个月后(D)。
患者在接受了创新性的自体NK细胞免疫治疗后,不仅症状得到了显著改善,而且生活质量也有了显著提升。这一治疗方法的成功,为肺癌治疗领域带来了新的希望。
治疗过程简述如下:首先从患者外周静脉抽取了20毫升血液,并通过先进的Ficoll密度梯度离心法提取出免疫细胞。这些细胞在富含IL-2、IL-12和IL-18的培养基中培养、激活并增殖。经过21天的培养,细胞数量达到了惊人的5×108个,其中NK细胞占比超过60%。重要的是,所有细胞样本均经过严格的安全评估,确保无细菌、支原体和内毒素污染。
患者在接下来的4.5个月内,每3周接受一次NK细胞输注,共进行了6次疗程。同时,他还接受了吉西他滨和贝伐单抗的联合化疗,每3周一次,连续进行了两个周期。令人振奋的是,经过这一综合治疗,患者的干咳、胸痛症状完全消失,食欲明显改善,生活质量得到了显著提升。更令人欣喜的是,在治疗过程中,患者并未出现明显的副作用,其肝功能和肾功能也保持在正常范围内。
更为关键的是,通过定期的PET/CT扫描显示,与治疗前相比,患者的主要肿瘤大小显著减小,纵隔和双侧锁骨上的淋巴结也未见踪影。这些影像学上的改善,进一步证实了自体NK细胞免疫治疗在肺癌治疗中的巨大潜力。
这一成功案例不仅为患者带来了新生,也为医学界提供了宝贵的实践经验。随着对NK细胞生物学和功能的深入研究,相信未来会有更多患者从中受益。
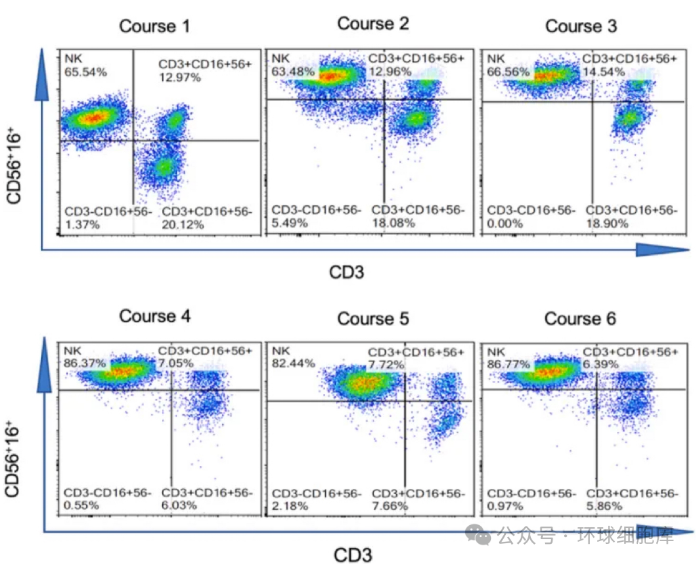
图4. NK细胞治疗的免疫表型监测。患者从2020年10月开始接受细胞治疗。患者接受了6个治疗疗程(每个疗程1次输注)的NK细胞治疗,治疗持续了4.5个月。每隔3周进行1次输注,共6次输注。
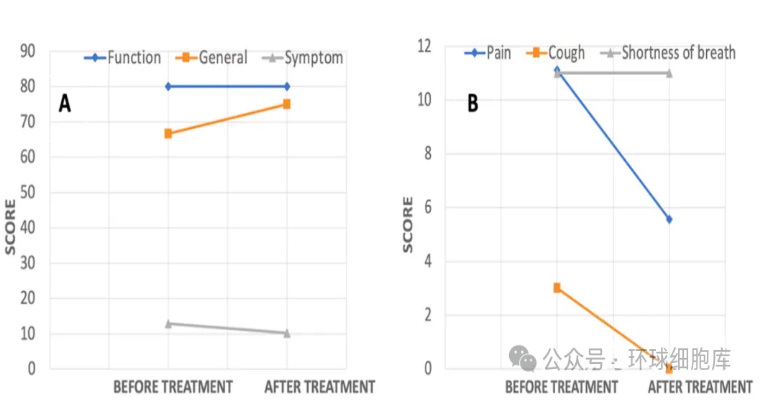
图5. 治疗前后患者生活质量的评估。A. 生活质量:患者整体情况较之前更好,症状明显减轻。B. 功能症状:经过6次输注后,患者的疼痛和咳嗽明显减轻。
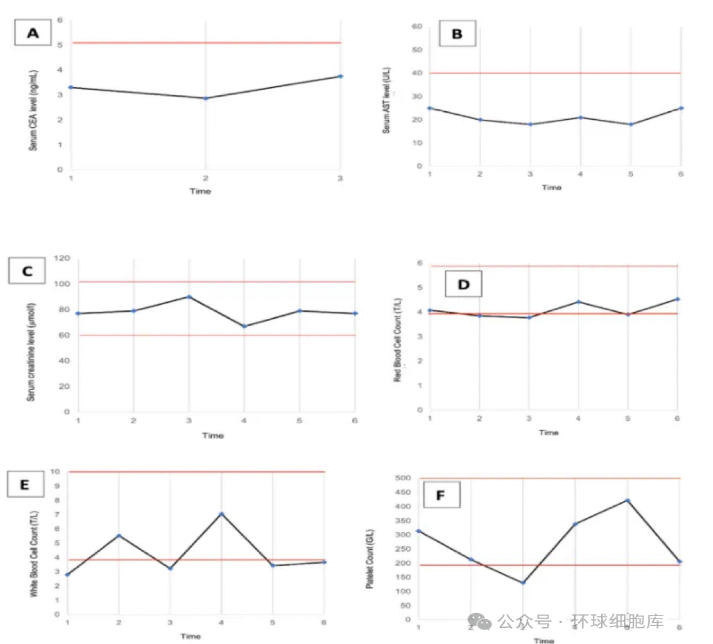
图6. 血液生化检查。大多数生化指标:CEA、AST、肌酐在NK细胞治疗前后保持在正常水平。红细胞、白细胞和血小板在治疗期间有时略低于正常水平。A. CEA、B. AST、C. 肌酐、D. 红细胞、E. 白细胞、F. 血小板。
小结
随着免疫学研究的深入,NK细胞疗法已成为癌症治疗领域的一颗璀璨新星,尤其在肺癌治疗中展现出巨大潜力。这种治疗方法的核心在于利用NK细胞——一种在免疫系统中发挥关键作用的细胞,具有识别和摧毁癌症干细胞的独特能力。
NK细胞表面上的CD16标记物使它们能够与IgG1、IgG3的Fc区域结合,进而引发抗体依赖性细胞毒作用(ADCC)。这意味着当NK细胞被注入患者体内时,它们不仅能直接攻击癌细胞,还能激发其他免疫细胞参与抗癌战斗。
最新研究显示,NK细胞疗法在抑制癌细胞增殖方面效果显著,从而降低了癌症复发和转移的风险。这一发现对于晚期非小细胞肺癌(NSCLC)患者来说尤为重要。一些研究表明,在接受帕博利珠单抗治疗的同时加入NK细胞疗法的患者,其生存期明显长于仅接受帕博利珠单抗治疗的患者。而且,多次NK细胞输注的患者组总体生存率(OS)也优于单次输注的患者组。
在针对EGFR突变的晚期肺腺癌的临床试验中,NK细胞治疗组的血清CEA和CA125水平显著低于非NK治疗组,且缓解率明显高于对照组。这些数据进一步证实了NK细胞疗法在肺癌治疗中的有效性和潜力。
随着研究的深入和技术的不断完善,NK细胞疗法有望为更多肺癌患者带来希望和新生。
参考资料:Nguyen TMT, Van Tran K, Ta VT, Tran LM, Tran CK, Trinh HL, Ta DT, Nguyen BT, Tran TH. A case of response to combination treatment with autologous immunotherapy and bevacizumab in advanced non-small cell lung cancer. Respir Med Case Rep. 2022 Dec 29;42:101804. doi: 10.1016/j.rmcr.2022.101804. PMID: 36845645; PMCID: PMC9945779.
申明:本公众号所发布的图片及内容,部分来源于国内外知名杂志及互联网,如内容涉及版权等问题,请立即联系管理员,我们会予以更改或删除相关文章,保证您的权利。


